


Visitas científicas:
Fevereiro-Março 2024: Prof. Romain
Os canais receptores de potencial transitório (TRP) são canais que mediam um variedade de sensações como dor, temperatura, frio, calor, pressão e visão. Estes canais são a base do sensoriamento dos seres humanos. Entender os TRP canais nos faz compreender como interpretamos o mundo.









Registro da corrente elétrica (faixa de 10-20 pA) de voltage clamp (-40 mV) realizado durante o curso prático do prof. Romain. Estes registros elétricos dos canais iônicos foram realizados pelos participantes em fibroblastos. (A) Explicação do prof. Romain do gráfico da corrente no tempo dos canais iônicos. (B) Histograma do valor das correntes elétricas de um voltage clamp. (C) Ampliação da tela do histograma. Essa informação pode ser usada para verificar quantos canais foram medidos. E também para calcular a probabilidade de um canal estar aberto. Eixo Y é o número de ocorrências, e eixo X a corrente.
Abril 2024: profa. Silvia Conde (Portugal) stay at IBIOCEL .
Fundamentals in the evaluation and management of cadiometabolic health: training on electrophysiology by extracellular measurements.

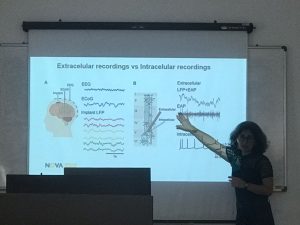



Os corpos carotídeos são classicamente descritos como sensores de O2 e CO2, mas que mais recentemente foram descritos como sensores metabólicos, capazes de sentir a composição química do nosso sangue, incluindo hormonas como a insulina e a leptina. Na ultima década descreveu-se que estes órgãos estão disfuncionais na diabetes e que a modulação da sua atividade pode ser um importante alvo terapêutico para tratar as doenças metabólicas como a obesidade e a diabetes. Os estudos eletrofisiológicos extracelulares dos corpos carotídeos podem nos fornecer informações importantes quer para entender o grau de disfunção destes órgãos nas diversas patologias metabólicas como para procurar diversos alvos moleculares para diminuir a sua atividade.
Bioelectronic modulation of carotid sinus nerve activity in the rat: a potential therapeutic approach for type 2 diabetes. Sacramento JF, Chew DJ, Melo BF, Donegá M, Dopson W, Guarino MP, Robinson A, Prieto-Lloret J, Patel S, Holinski BJ, Ramnarain N, Pikov V, Famm K, Conde SV. Diabetologia. 2018 Mar;61(3):700-710. doi: 10.1007/s00125-017-4533-7.
Conde SV, Sacramento JF, Melo BF, Fonseca-Pinto R, Romero-Ortega MI, Guarino MP. Blood Pressure Regulation by the Carotid Sinus Nerve: Clinical Implications for Carotid Body Neuromodulation. Front Neurosci. 2022 Jan 10;15:725751. doi: 10.3389/fnins.2021.725751. PMID: 35082593; PMCID: PMC8784865.
Junho 2024: dr. Andre Luiz Andreotti Dagostin
Senior Research Associate in the von Gersdorff lab at the Vollum Institute (Oregon Health and Science University)
Recording electrical signals from cells: how and why?



Práticas de eletrofisiologia



Estudo de INS-1 832/13 Rat Insulinoma Cell Line
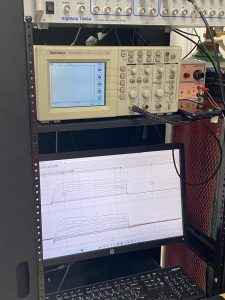
Estímulos de voltagem de intensidades diferentes são aplicadas em células INS-1 832/13, na tela está a resposta dos canais iônicos com aumento da corrente para o aumento dos estímulos elétricos.
A linhagem celular de insulinoma de rato INS-11 é um modelo bem estabelecido para estudos da função das células beta das ilhotas pancreáticas; no entanto, a resposta à GSIS das células INS-1 pode diminuir ao longo do tempo. A linha celular INS-1 832/13 é um subclone de INS-1 que foi selecionado para GSIS robusta, produzindo e secretando tanto insulina de rato quanto humana. INS-1 832/13 possui um cassete de expressão de insulina humana que permite a secreção de insulina humana ser mantida ao longo de passagens prolongadas com seleção. As células INS-1 832/13 exibem uma responsividade secretora aprimorada à glicose em comparação com a linha celular parental INS-1. As células INS-1 832/13 podem ser caracterizadas por coloração granular para sinaptotagmina, como descrito para a linha celular parental. Essas características tornam as células INS-1 832/13 um sistema útil para investigar os mecanismos de secreção, armazenamento e síntese de insulina celular.
Por que estudar células beta das ilhotas pancreáticas?
As células beta pancreáticas são um tipo de célula presente nas ilhotas pancreáticas, também conhecidas como ilhotas de Langerhans. Elas são responsáveis pela produção e secreção do hormônio insulina. A insulina desempenha um papel fundamental no controle dos níveis de glicose no sangue. Quando os níveis de glicose no sangue aumentam após uma refeição, as células beta pancreáticas respondem secretando insulina. A insulina então ajuda as células do corpo a absorver a glicose do sangue, permitindo que elas a utilizem como fonte de energia ou armazenem-na para uso futuro. Esse processo é essencial para manter os níveis de glicose no sangue dentro de uma faixa normal e para garantir o fornecimento de energia adequado às células do corpo. Quando as células beta pancreáticas não funcionam adequadamente, isso pode levar a condições como diabetes mellitus, onde os níveis de glicose no sangue se tornam desregulados.
O que é GSIS?
GSIS é a sigla para “Glucose-Stimulated Insulin Secretion” (Secreção de Insulina Estimulada por Glicose, em tradução livre). Refere-se ao processo pelo qual as células beta pancreáticas secretam insulina em resposta ao aumento dos níveis de glicose no sangue. Quando a concentração de glicose no sangue aumenta, especialmente após uma refeição, as células beta pancreáticas detectam esse aumento e respondem secretando insulina. A insulina então ajuda a reduzir os níveis de glicose no sangue, facilitando sua absorção pelas células do corpo. Esse processo é vital para manter a homeostase da glicose e garantir que os tecidos do corpo recebam a quantidade necessária de energia. Estudar a GSIS é fundamental para entender melhor os mecanismos subjacentes ao controle dos níveis de glicose no sangue e pode ter implicações importantes para o tratamento de distúrbios metabólicos, como o diabetes mellitus.
Por que usar eletrofisiologia para estudar células beta das ilhotas pancreáticas ?
- Avaliação da atividade elétrica celular: As células beta pancreáticas possuem atividade elétrica que desempenha um papel crucial na regulação da secreção de insulina. A eletrofisiologia permite registrar e analisar essa atividade elétrica, incluindo potenciais de membrana, correntes iônicas e oscilações de cálcio, fornecendo informações detalhadas sobre os mecanismos subjacentes à secreção de insulina.
- Estudo de canais iônicos: Os canais iônicos desempenham um papel essencial na regulação da atividade elétrica das células beta pancreáticas e, consequentemente, na secreção de insulina. A eletrofisiologia permite caracterizar e entender melhor a função desses canais, incluindo sua condutância, cinética e modulação por diferentes estímulos, como a glicose.
- Investigação de mecanismos de secreção de insulina: A eletrofisiologia pode ser usada para estudar os eventos bioelétricos que precedem e acompanham a secreção de insulina, ajudando a elucidar os mecanismos envolvidos na regulação desse processo complexo.
- Avaliação de drogas e compostos: A eletrofisiologia pode ser usada para testar o efeito de diferentes drogas e compostos na atividade elétrica e na secreção de insulina das células beta pancreáticas. Isso é crucial para o desenvolvimento de novos tratamentos para distúrbios metabólicos, como o diabetes mellitus.
Em resumo, a eletrofisiologia oferece uma abordagem poderosa e detalhada para investigar a fisiologia das células beta pancreáticas, ajudando a expandir nosso entendimento sobre a regulação da secreção de insulina e o funcionamento do pâncreas endócrino.
Este estudo é aplicado a entender que tipo de doença?
A não regulação adequada da secreção de insulina está fortemente ligada a condições como o diabetes mellitus, uma das principais doenças metabólicas em todo o mundo. Existem diferentes tipos de diabetes mellitus, incluindo o tipo 1 e o tipo 2, ambos com ligações à secreção de insulina:
- Diabetes Mellitus Tipo 1 (DM1): Neste tipo de diabetes, o sistema imunológico ataca e destrói as células beta pancreáticas, responsáveis pela produção e secreção de insulina. Como resultado, há uma produção insuficiente de insulina, levando a níveis elevados de glicose no sangue (hiperglicemia). A regulação prejudicada da secreção de insulina é a principal característica do DM1.
- Diabetes Mellitus Tipo 2 (DM2): No DM2, as células beta pancreáticas podem inicialmente produzir insulina em quantidades normais ou até mesmo aumentadas. No entanto, as células do corpo se tornam menos sensíveis à ação da insulina (resistência à insulina), exigindo que o pâncreas produza mais insulina para manter os níveis de glicose no sangue dentro da faixa normal. Com o tempo, a capacidade das células beta pancreáticas de produzir insulina pode diminuir, contribuindo para a progressão do DM2.
Além do diabetes mellitus, outras condições podem estar associadas a distúrbios na regulação da secreção de insulina, como síndromes genéticas raras e tumores do pâncreas, que podem afetar as células beta ou interferir nos mecanismos de controle da secreção de insulina.
Treinamento de Análise Histológicas-Profa. Kieiv Resende Sousa de Moura
A Profa. Kieiv Resende Sousa de Moura do departamento de Ciências Morfológicas da UFSC e colaboradora do IBIOCEL. – Outubro 2024
As análises histológicas proporcionam o estudo detalhado da estrutura das células e tecidos biológicos, permitindo verificar a ocorrência de alterações morfológicas decorrentes de modificações fisiológicas e fatores experimentais. As técnicas histológicas, como as colorações de rotina e a imuno-histoquímica, possibilitam a visualização de componentes celulares específicos, aumentando a precisão dos experimentos e fornecendo dados sobre a localização e quantidade de moléculas específicas, essenciais no entendimento dos mecanismos moleculares e celulares.


 Conferência via CAPES/PrINT na Medical School – Universidade Nova de Lisboa
Conferência via CAPES/PrINT na Medical School – Universidade Nova de Lisboa

Em 16 de outubro de 2024, a Profª. Fátima esteve na Universidade Nova de Lisboa em encontro com a Profª. Silvia Conte. O objetivo da visita foi fortalecer a internacionalização de instituições de ensino superior brasileiras, fomentando a pesquisa, a mobilidade acadêmica e a criação de redes internacionais.
Treinamento no micrótomo IBIOCEl Prof. Gabriel Leite
O Prof. Gabriel Leite do Departamento de Biologia Celular, Embriologia e Genética da UFSC e colaborador do IBIOCEL. – Agosto 2024.
Treinamento no Micrótomo: Preparação de Amostras com Precisão
O treinamento no uso do micrótomo é essencial para quem trabalha com análise de tecidos biológicos, permitindo a obtenção de cortes ultrafinos e uniformes para observação em microscopia. Este equipamento é amplamente utilizado em laboratórios de histologia, patologia e pesquisa biomédica.
Objetivos do Treinamento
- Familiarização com o Equipamento: Entender a estrutura e o funcionamento do micrótomo, incluindo ajuste de lâminas, controle de espessura e segurança.
- Preparação de Amostras: Aprender técnicas adequadas de inclusão em parafina ou resina para garantir cortes de alta qualidade.
- Técnicas de Corte: Dominar o processo de seccionar amostras com precisão, evitando danos ao tecido e desperdício de material.
- Manutenção e Cuidados: Garantir o uso adequado e a conservação do equipamento para prolongar sua vida útil.
Benefícios do Treinamento
- Qualidade nas Análises: Cortes consistentes e precisos são fundamentais para observações detalhadas em microscopia óptica ou eletrônica.
- Eficiência no Laboratório: Reduz desperdícios e otimiza o tempo de preparo das amostras.
- Segurança: O uso correto do micrótomo minimiza riscos de acidentes com lâminas afiadas.
- Desenvolvimento Profissional: Adquirir essa habilidade técnica é um diferencial em áreas como biologia, medicina e engenharia biomédica.
O treinamento é ideal para pesquisadores, técnicos e estudantes que buscam aprimorar suas habilidades no preparo de amostras para análise microscópica. A prática e o domínio dessa técnica são passos importantes para resultados confiáveis e precisos.




Curso com a profa. Eloisa da Silveira Loss (UFRGS)
Foi realizado entre 22 a 31 de Janeiro de 2025 no IBIOCEL o curso:
Ação Hormonal na Membrana Plasmática: Uma abordagem eletrofisiológica





Registros de correntes em células 3T3L1 IBIOCEL

profa. Eloísa supervisionando os participantes do curso na prática da eletrofisiologia no IBIOCEL.

Célula de pré-adipócito e a micropipeta de vidro inserida na célula.
Tópicos abordados abordaram aspectos teóricos e práticos da ação hormonal e sua relação com a eletrofisiologia:
1. Introdução à Eletrofisiologia e Ação Hormonal
2. Membrana Plasmática e Mecanismos de Sinalização
3. Canais Iônicos e Efeitos Hormonais
4. Técnicas Eletrofisiológicas Aplicadas ao Estudo Hormonal
5. Estudos de Caso: Ação Hormonal Mediada por Efeitos Bioelétricos
6. Dinâmica de Sinalização Hormonal em Diferentes Tipos Celulares
7. Interpretação de Dados Eletrofisiológicos
8. Aplicações Clínicas e Terapêuticas
9. Prática Experimental com equipamento de Patch Clamp
10. Discussão de Trabalhos Científicos
Curso de Cultivo Celular: Principais Dúvidas
profa. Carine Royer

Entre 10 a 14 de de Fevereiro de 2025
O curso é direcionado a estudantes e profissionais da área de farmácia, biologia, biomedicina, engenharia biomédica e afins, abordando temas essenciais como introdução ao cultivo celular, infraestrutura e equipamentos necessários, preparo de meios de cultura e suplementos, técnicas básicas de cultivo (subcultivo e criopreservação), prevenção de contaminações, aplicações na pesquisa e indústria, além de solução de problemas comuns e tendências inovadoras na área. O objetivo é esclarecer dúvidas frequentes e fornecer conhecimentos práticos para otimizar o trabalho com células, garantindo qualidade e eficiência no laboratório.

















































